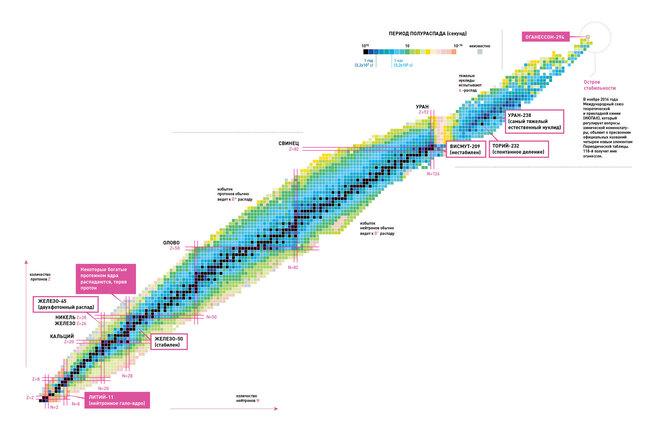
Límits de la taula periòdica dels elements. On és la feliç illa de l'estabilitat?
La taula periòdica dels elements té un límit "superior"; per tant, hi ha un nombre atòmic teòric per a un element superpesat que seria impossible d'assolir al món físic conegut? El físic rus Yuri Oganesyan, del qual s'anomena l'element 118, creu que aquest límit ha d'existir.
Segons Oganesyan, cap del laboratori Flerov del Joint Institute for Nuclear Research (JINR) de Dubna, Rússia, l'existència d'aquest límit és el resultat d'efectes relativistes. A mesura que augmenta el nombre atòmic, la càrrega positiva del nucli augmenta, i això, al seu torn, augmenta la velocitat dels electrons al voltant del nucli, apropant-se al límit de velocitat de la llum, explica el físic en una entrevista publicada al número d'abril de la revista. . Científic nou. "Per exemple, els electrons més propers al nucli de l'element 112 viatgen a 7/10 de la velocitat de la llum. Si els electrons exteriors s'apropessin a la velocitat de la llum, canviaria les propietats de l'àtom, violant els principis de la taula periòdica", diu.
Crear nous elements superpesants als laboratoris de física és una tasca tediosa. Els científics han d'equilibrar, amb la màxima precisió, les forces d'atracció i repulsió entre partícules elementals. El que es necessita és un nombre "màgic" de protons i neutrons que "s'enganxin" al nucli amb el nombre atòmic desitjat. El procés en si accelera les partícules a una desena part de la velocitat de la llum. Hi ha una petita, però no zero, possibilitat de formació d'un nucli atòmic superpesat del nombre requerit. Aleshores, la tasca dels físics és refredar-lo el més ràpid possible i "atrapar-lo" al detector abans que es decai. Tanmateix, per a això cal obtenir les "matèries primeres" adequades: isòtops d'elements rars i extremadament cars amb els recursos de neutrons necessaris.
Essencialment, com més pesat sigui un element del grup dels transactínids, més curta serà la seva vida útil. L'element amb nombre atòmic 112 té una vida mitjana de 29 segons, 116 - 60 mil·lisegons, 118 - 0,9 mil·lisegons. Es creu que la ciència arriba als límits de la matèria físicament possible.
No obstant això, Oganesyan no està d'acord. Presenta el punt de vista que es troba en el món dels elements superpesants. "Illa de l'estabilitat". "El temps de desintegració dels nous elements és extremadament curt, però si afegiu neutrons als seus nuclis, la seva vida útil augmentarà", assenyala. "Afegir vuit neutrons als elements numerats 110, 111, 112 i fins i tot 113 allarga la seva vida 100 anys. un cop".
Rep el nom d'Oganesyan, l'element Oganesson Pertany al grup dels transactínids i té nombre atòmic 118. Va ser sintetitzat per primera vegada l'any 2002 per un grup de científics russos i nord-americans del Joint Institute for Nuclear Research de Dubna. El desembre de 2015, va ser reconegut com un dels quatre nous elements pel Joint Working Group IUPAC/IUPAP (grup creat per la Unió Internacional de Química Pura i Aplicada i la Unió Internacional de Física Pura i Aplicada). La denominació oficial va tenir lloc el 28 de novembre de 2016. Oganesson ma nombre atòmic més alt i massa atòmica més gran entre tots els elements coneguts. El 2002-2005, només es van descobrir quatre àtoms de l'isòtop 294.
Aquest element pertany al grup 18 de la taula periòdica, és a dir. gasos nobles (siendo el seu primer representant artificial), però, pot mostrar una reactivitat important, a diferència de tots els altres gasos nobles. En el passat, es pensava que l'oganesson era un gas en condicions estàndard, però les prediccions actuals apunten a un estat d'agregació constant en aquestes condicions a causa dels efectes relativistes que Oganessian va esmentar a l'entrevista citada anteriorment. A la taula periòdica, es troba al bloc p, sent l'última arrel del setè període.
Històricament, tant els estudiosos russos com els nord-americans han proposat diferents noms per a ella. Al final, però, la IUPAC va decidir honrar la memòria d'Hovhannisyan reconeixent la seva gran contribució al descobriment dels elements més pesats de la taula periòdica. Aquest element és un dels dos (al costat del seaborg) que porten el nom d'una persona viva.

